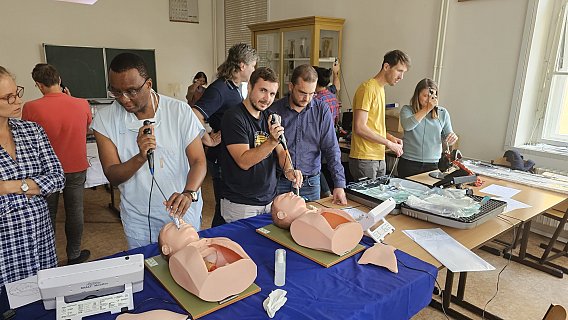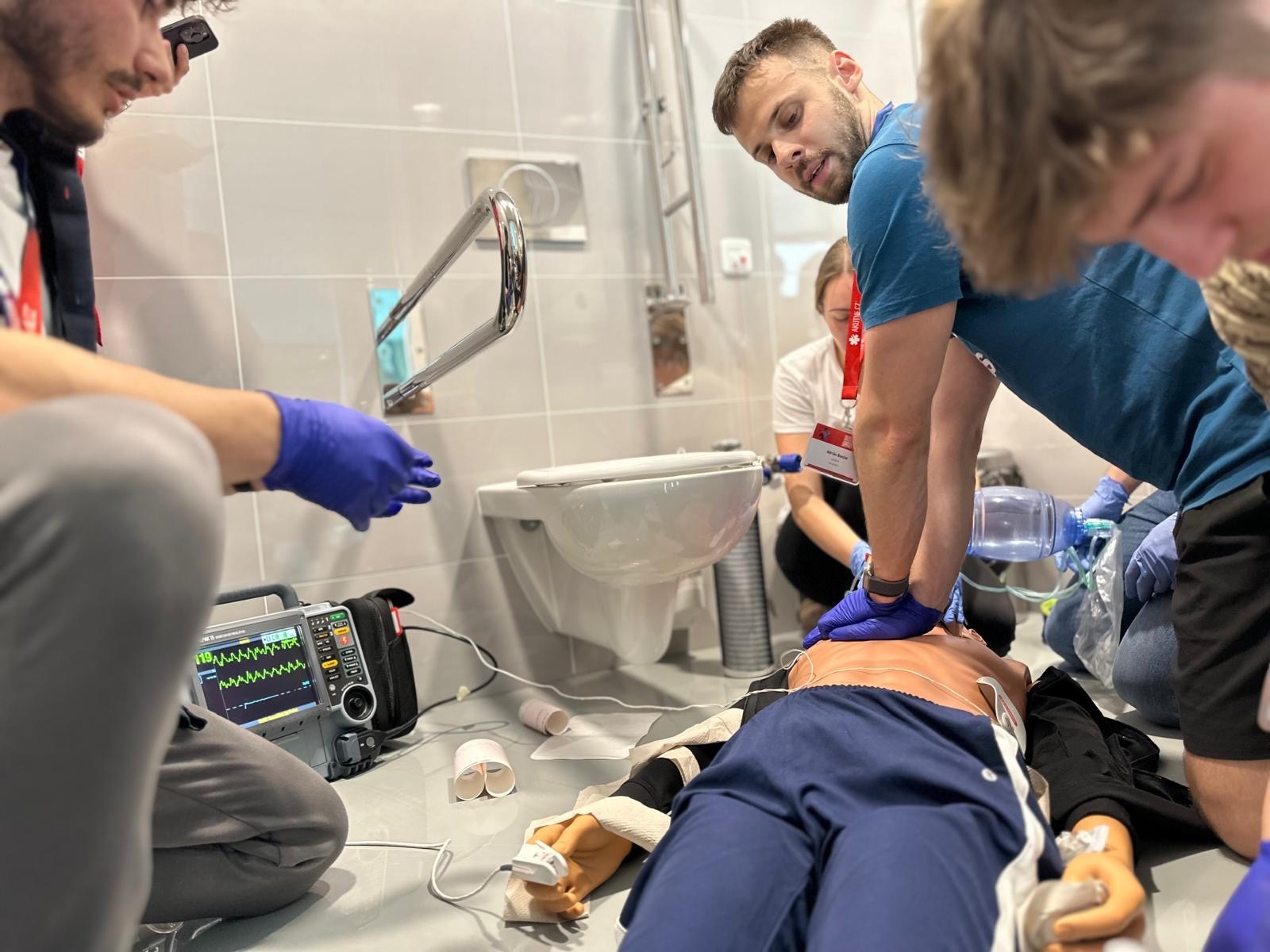
Kurz urgentní medicíny 2024
Po roce se do Simulačního centra LF MU vrátil Kurz urgentní medicíny, který se letos konal 13. dubna 2024. Tradiční kurz, pořádaný portálem AKUTNĚ.CZ pro studenty 4.- 6. ročníku Všeobecného lékařství LF MU, se konal již potřetí v novém hávu a v jednom z nejmodernějších pracovišť simulované výuky.